大叔John,60岁,2021年他背部上胸椎区出现隐痛。在医院拍了X光、脊柱MRI检查,结果提示存在骨病变。
医生在体格检查时发现,John的左侧眼球突出,眶内异位,左眼低于右眼。视力为6/36,针孔试验6/18。John告诉医生,自己30年前因左眼问题看眼科医生,那时医生表示这是外貌问题,不用治疗。
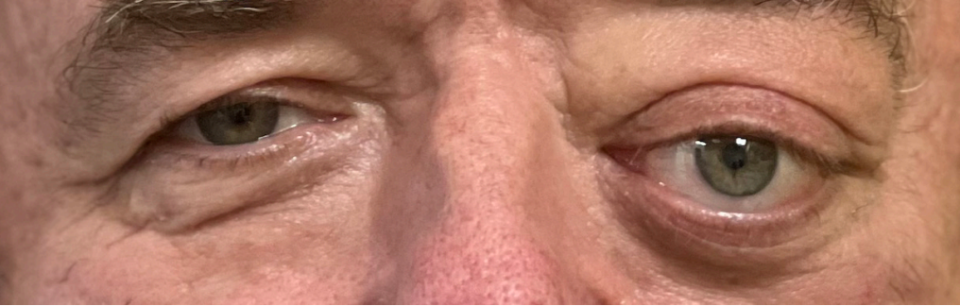
医生为他安排了影像学检查,CT提示,T3椎体溶解性病变;多发肺部病变,考虑转移。多发肺部病变。脊柱MRI提示,胸椎上段病变,伴T3塌陷及椎管狭窄。T3塌陷及椎管狭窄,MRI示脑内浸润,集中于左侧眶上区,考虑浸润性脑膜瘤;硬脑膜突出,提示脑脊液漏。
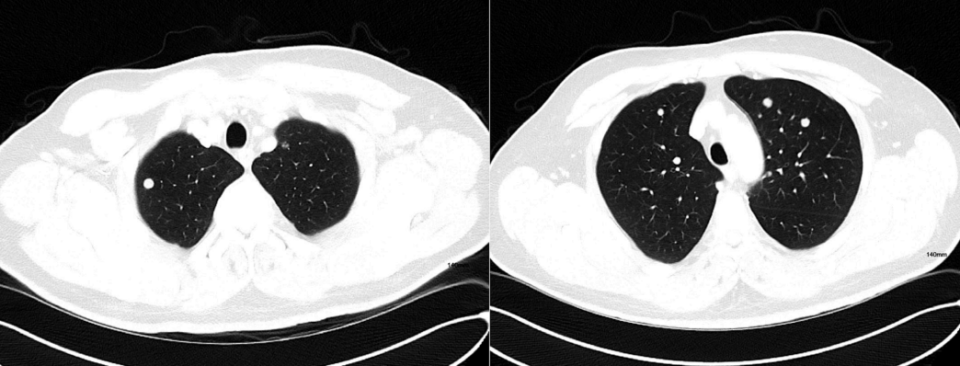
CT示多发肺部病变
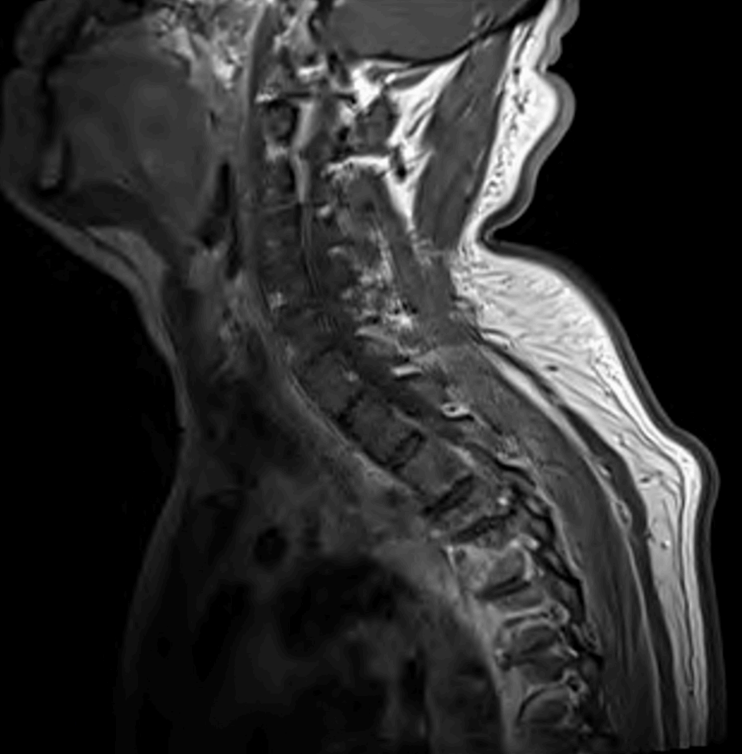
MRI示T3塌陷及椎管狭窄
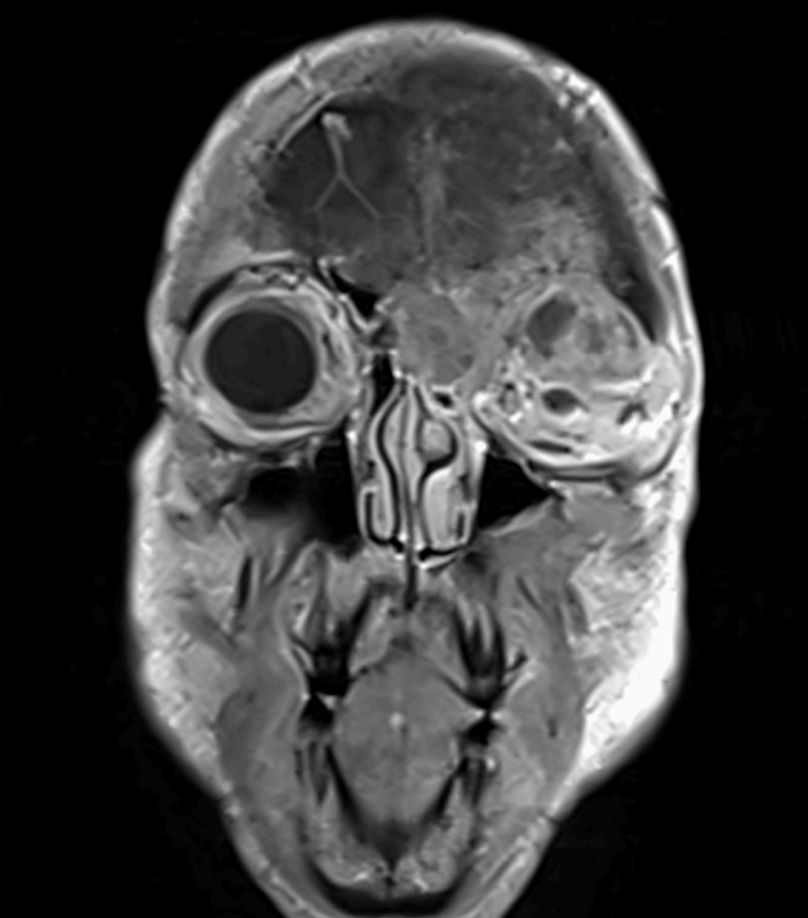
颅内MRI示颅底肿块伴浸润
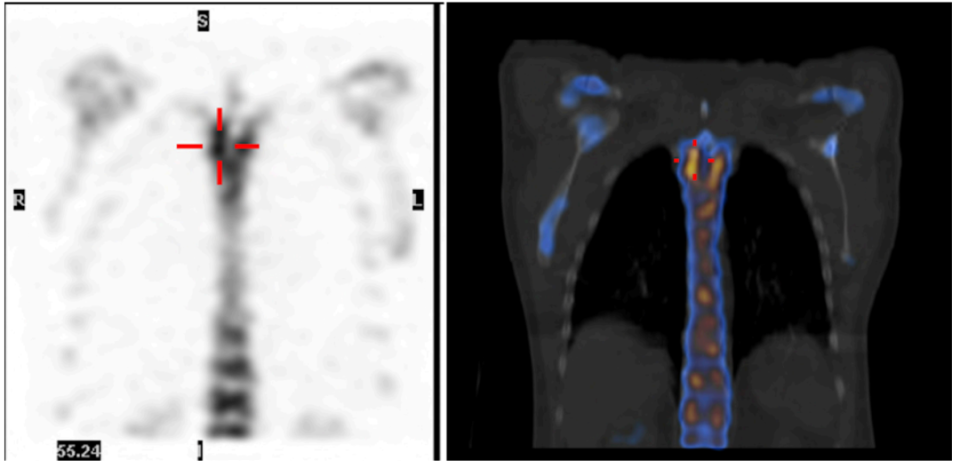
骨扫描和SPECT/CT示多发转移灶
颅内MRI示颅底肿块伴浸润,骨扫描和SPECT/CT示额部、眶部及T3椎体、T8椎体多发病灶。骨扫描和SPECT/CT示多发转移灶。
对左侧眼眶处肿块进行活检。活检示中分化腺癌,考虑起源于泪腺。此外,在一个小唾液腺附近发现了筛状病变。医生结合John的临床表现诊断为HER2阳性泪腺/唾液腺导管腺癌,伴多发转移。
医生考虑到John脊柱存在转移病灶,且有骨折风险,建议他开始佩戴颈圈以固定脊柱。
随后,针对全身转移病灶,John接受了姑息化疗、放疗。活检结果显示肿瘤组织HER2高表达,因此患者还接受了抗HER2靶向治疗。药物治疗方案包括唑来膦酸、曲妥珠单抗、紫杉醇。
考虑到John长期的背部隐痛,予以止痛药控制。不幸的是,诊断后的6个月,患者出现视力下降,并出现视神经压迫症状。
原发性泪腺导管腺癌是一种极罕见的上皮源性恶性肿瘤,1996 年由 Katz 首先报道。其临床病理特征仍不明确,侵袭性强,因肿瘤早期临床症状较轻,就诊时多已属于晚期,且影像学缺乏特异性征象,容易误诊,预后差。泪腺肿瘤的发病率极低,每年大约每百万人中一人被诊断患有这种肿瘤。
临床表现
泪腺肿瘤通常发生在上眼睑,患者可能没有症状,也可能出现眼球突出、视力下降等眼部症状。若临床表现为可触及的肿块、生长迅速、眼球突出、疼痛和视力下降等,但病变早期通常症状较轻,导致就诊时多属于晚期,发生远处转移,则相应组织器官可能出现症状。
原发性泪腺导管癌主要发生在男性,约占73%,以突出眼、视力下降为常见的表现症状。发病早期即有局部和远处转移的倾向,且局部复发率高。淋巴结转移较常见,常见的转移部位包括颈部淋巴结(31%)、骨(23%)、脑(23%)、肺(23%)和肝脏(15%),大多数患者于确诊后3年内死亡。
诊断
诊影像上表现为恶性征象,不规则肿块,骨质侵蚀破坏,病灶内有局部钙化。病理检查可做出准确判断,由于泪腺的原发性导管腺癌非常罕见,目前仅有少数的标记物被报道,崔红光等通过对 13 篇文献进行分析,认为 GCDFP15、AR及 Her-2 可以作为原发性泪腺导管腺癌的特征性免疫组化指标,并推荐对泪腺区肿瘤的患者常规检测这 3个指标。田梦等认为 GCDFP-15、Her-2、CK5/6、CK7 均为乳腺导管腺癌及唾液腺的指标,并发现既往病例报道中这些指标都表达为阳性。
组织病理检查提示,该肿瘤中导管内癌样成分与乳腺的导管癌有相似之处,这也正是它有别于其他涎腺恶性肿瘤之处。导管内癌成分有3种表现,乳头状、粉刺状和筛孔状结构。浸润性成分可表现为乳头状或无特殊结构。肿瘤细胞大,核深染并呈多形性,少数可见明显核仁。细胞质中等,呈嗜酸性。核分裂常见。少数标记物被报道:EMA、基质金属蛋白酶-2、9、13,细胞角蛋白7和人类表皮生长因子受体2。
免疫组织化学染色表现为细胞角蛋白-7、癌胚抗原、上皮膜抗原、巨囊病囊液蛋白、雄激素受体等呈阳性染色,而平滑肌肌动蛋白染色呈阴性。高侵袭力的肿瘤常表现为HER-2/neu阳性染色。若全身检查未发现其他原发性恶性肿瘤,结合组织病理学检查和免疫组织化学染色结果可确诊为泪腺导管腺癌。
该病的影像学检查主要包括CT、MRI以及PET/CT等,其中CT和MRI检查缺乏特异性,易误诊为良性肿瘤。PET/CT有助于全身受累情况的判断,但由于其费用昂贵,目前尚未普及。
影像上恶性征象:不规则肿块,骨质侵蚀,病灶内有局部钙化。需要注意的是,原发性腺癌也会表现为边界清晰,有囊性病变,误导诊断为良性。
治疗
原发性泪腺导管腺癌恶性程度高、易转移复发,一经确诊应该立即根治性手术切除病变、淋巴结清扫并术后辅助大剂量放疗,防止疾病进一步发展。但如果患者已经存在远处转移,局部治疗效果欠佳,则需要联合全身治疗,如化疗、靶向治疗。
对于HER2高表达的肿瘤,如乳腺癌、胃癌、食管癌等,使用HER2靶向药物可以有效控制肿瘤进展,改善预后。但是,抗HER2治疗在泪腺癌/唾液腺癌的治疗数据有限。
此前,有个例报道显示,拉帕替尼治疗HER2阳性唾液腺患者表现出较好的疗效。一项研究发现,晚期或转移性HER2阳性唾液腺癌患者使用曲妥珠单抗的活性差,因此需要联合其他药物治疗。
日本一项研究纳入了57例晚期HER2阳性唾液腺癌患者的II期临床研究显示,曲妥珠单抗联合多西他赛治疗的有效率达70%。而另一项晚期唾液腺癌靶向治疗的IIa期篮子研究显示,使用帕妥珠单抗/曲妥珠单抗治疗HER2扩增/过表达晚期唾液腺癌可有较好的疗效。
维迪西妥单抗(disitamab vedotin,RC48)是首款由中国自主研发的抗体偶联药物(ADC),已被批准用于至少接受过 2 个系统化疗的 HER2 过表达局部晚期或转移性胃癌(包括胃食管结合部腺癌)的患者。在治疗前应使用 NGS 分析和其他适当的生物标记物检测来检查雄激素受体、HER2、NTRK 等,临床医生可依据肿瘤分子改变选择相应的靶向药物治疗。
恩美曲妥珠单抗(T-DM1)可作为二线治疗,用于含曲妥珠单抗治疗失败的患者,其他后线治疗方案大多效果欠佳。DS-8201 是是阿斯利康 & 第一三共制药联合研发的一款靶向 HER2 的抗体偶联 (ADC) 药物, 在赫赛汀耐药后的 SDC 脑转移中有效的病例报道。